INSTITUTO NACIONAL DE SEMILLAS
Resolución 428/2015
Bs. As., 20/10/2015
VISTO el Expediente N° S05:0041549/2014 y la Resolución N° 217 de fecha
29 de octubre de 2002 de la entonces SECRETARÍA DE AGRICULTURA,
GANADERÍA, PESCA Y ALIMENTOS, y la Resolución N° 164 de fecha 28 de
septiembre de 2004 del INSTITUTO NACIONAL DE SEMILLAS, organismo
descentralizado actuante en la órbita del MINISTERIO DE AGRICULTURA,
GANADERÍA Y PESCA, y
CONSIDERANDO:
Que a los fines de resguardar la sanidad de los tubérculos de papa
empleados como material de propagación, es necesario mantener
actualizada la normativa referente a la habilitación y funcionamiento
de Laboratorios de Análisis de Papa Semilla que certificarán dicha
sanidad.
Que las condiciones que debe reunir un laboratorio y las normas para su
funcionamiento dependen de los análisis y del material que pretenda
analizar.
Que la presente norma complementa la Resolución de la entonces
SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS N° 217 de fecha
29 de octubre de 2002 referida a las “NORMAS DE PRODUCCIÓN DE PAPA
SEMILLA EN CONDICIONES CONTROLADAS” y las “NORMAS PARA LA FISCALIZACIÓN
DE PAPA SEMILLA EN CAMPO”.
Que en virtud del Artículo 13 de la Ley N° 20.247, los laboratorios de
análisis deben estar inscriptos en el Registro Nacional del Comercio y
Fiscalización de Semillas.
Que por el Artículo 1 de la Resolución N° 42 de fecha 6 de abril de
2000 y su respectivo Anexo I se crean categorías que contemplan a los
laboratorios.
Que por los Artículos 2° y 3° de la mencionada Resolución y en sus
respectivos Anexos II, III y IV se establece que los laboratorios
deberán cumplir previamente a su inscripción, con normas establecidas
en la materia.
Que a los efectos de dar cumplimiento a la Resolución N° 217 de la
entonces SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS de
fecha 29 de octubre de 2002, es necesario contar con laboratorios y
establecer protocolos de habilitación a los cuales los mismos se
deberán ajustar para inscribirse.
Que la Dirección de Calidad, la Dirección de Certificación y Control y
la Dirección de Asuntos Jurídicos, pertenecientes al INSTITUTO NACIONAL
DE SEMILLAS, organismo descentralizado actuante en la órbita del
MINISTERIO DE AGRICULTURA, GANADERÍA Y PESCA, han tomado la
intervención técnica que les compete.
Que la COMISIÓN NACIONAL DE SEMILLAS, creada por la Ley de Semillas y
Creaciones Fitogenéticas N° 20.247, se ha pronunciado favorablemente
según surge del Acta N° 429 de fecha 14 de octubre de 2015.
Que el suscripto es competente para dictar el presente acto en virtud
de lo establecido en el Artículo 9° del Decreto N° 2.817 de fecha 30 de
diciembre de 1991, ratificado por la Ley N° 25.845.
Por ello,
EL PRESIDENTE DEL DIRECTORIO DEL INSTITUTO NACIONAL DE SEMILLAS
RESUELVE:
ARTÍCULO 1° — Apruébase las NORMAS DE FUNCIONAMIENTO DE LABORATORIOS DE
ANÁLISIS FITOSANITARIOS DE PAPA SEMILLA que como Anexos I a IV forman
parte integrante de la presente resolución.
ARTÍCULO 2° — Para comenzar el proceso de habilitación técnica del
laboratorio el interesado deberá presentar debidamente completados una
nota solicitando la habilitación, Datos del Laboratorio (Anexo I-A), el
Término de Compromiso del Director Técnico (Anexo I-B), el Listado de
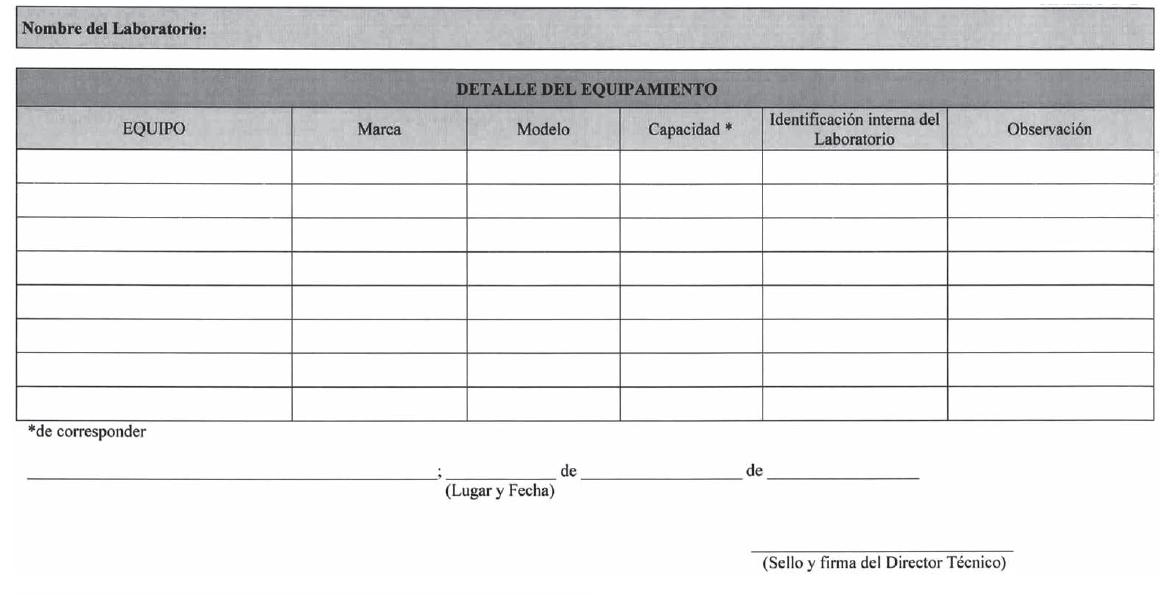
Analistas (Anexo I-C), el Detalle del Equipamiento (Anexo I-D) y el/los
Protocolo/s con su/s respectivo/s documento/s de adopción del método
según el alcance que solicita habilitar (Anexo II-A y/o Anexo II-B)
ante la Dirección de Calidad del INSTITUTO NACIONAL DE SEMILLAS,
organismo descentralizado actuante en la órbita del MINISTERIO DE
AGRICULTURA, GANADERÍA Y PESCA.
Toda documentación que no cumpla con los requisitos de fondo y de forma
exigidos en la presente norma será devuelta (de ser identificable su
autor) o desechada y se tendrá por nunca presentada.
ARTÍCULO 3° — La habilitación del Laboratorio de Análisis
Fitosanitarios de Papa Semilla estará condicionada a la aceptación de
la información presentada por el interesado, al título profesional del
postulante al cargo de Director Técnico y la capacitación específica
del mismo, a la disponibilidad del equipamiento mencionado en el Anexo
III de la presente resolución, a la aprobación de la auditoría de
habilitación, y al cumplimiento de los criterios y requisitos que el
INSTITUTO NACIONAL DE SEMILLAS establezca como necesarios.
ARTÍCULO 4° — El postulante al cargo de Director Técnico deberá contar
con título universitario oficial no menor de CUATRO (4) años con
incumbencia profesional o grados superiores de educación (con
incumbencia en la materia) y experiencia acreditable en el área técnica
correspondiente al alcance de la habilitación solicitada. Al inicio de
los trámites deberá presentar fotocopia del título profesional
habilitarte y fotocopia de la matrícula profesional —de corresponder—,
junto a un curriculum vitae actualizado y firmado, con sus respectivos
comprobantes.
De considerarlo necesario y bajo su entera responsabilidad podrá
nombrar un Reemplazante Autorizado. Para esta designación deberá
presentar debidamente completado ante la Dirección de Calidad la
Designación de Reemplazante Autorizado (Anexo I-E), firmado por el
autorizado y endosado por el Director Técnico.
ARTÍCULO 5° — El Reemplazante Autorizado deberá tener una capacitación
y un entrenamiento acorde al alcance de la habilitación. Deberá
presentar un curriculum vitae actualizado y firmado a modo de
Declaración Jurada.
ARTÍCULO 6° — Una vez obtenida la habilitación técnica otorgada por la
Dirección de Calidad el interesado deberá proceder a su inscripción
ante el Registro Nacional del Comercio y Fiscalización de Semillas en
un plazo razonable.
ARTÍCULO 7° — La Dirección de Calidad llevará a cabo la auditoría y el
control de los laboratorios inscriptos, estando obligado el Director
Técnico a estar presente en las auditorías y a brindar al INSTITUTO
NACIONAL DE SEMILLAS toda la documentación que requiera.
ARTÍCULO 8° — La falta de envío de las propuestas de acciones
correctivas para el levantamiento de no conformidades encontradas en la
auditoría dentro del plazo establecido por el auditor, hará pasible al
laboratorio de la aplicación de lo previsto por el Artículo 19.
ARTÍCULO 9° — En los casos que existan resultados cuestionados, la
Dirección de Calidad y/o la Dirección de Certificación y Control
intervendrán en los aspectos de su competencia.
ARTÍCULO 10. — Los certificados emitidos por los laboratorios
habilitados tendrán validez en el orden nacional y deberán ser
confeccionados conforme el modelo autorizado que se detalla en el Anexo
IV de la presente resolución.
Para ser válidos los certificados emitidos deberán contener sello y
firma del Director Técnico quien se hará responsable del contenido de
los mismos. Deberán estar debidamente completados no pudiendo contener
borrones ni enmiendas ni ser completados a mano. Bajo responsabilidad
del Director Técnico podrán ser firmados por el Reemplazante Autorizado
designado.
ARTÍCULO 11. — La Dirección de Calidad podrá solicitar a los
laboratorios copia firmada de los certificados emitidos y de cualquier
registro asociado a estos.
ARTÍCULO 12. — Todos los laboratorios habilitados deberán participar de
los ensayos interlaboratorios organizados por la Dirección de Calidad.
Conjuntamente a lo anterior, la Dirección de Calidad podrá convocar
tanto a los Directores Técnicos como a los analistas a jornadas,
talleres o cursos de capacitación.
ARTÍCULO 13. — Toda modificación en la situación del laboratorio en
cuanto a domicilio, instalaciones que afecten al desarrollo de ensayos,
protocolos, y/o Director Técnico, deberá comunicarse en forma
fehaciente a la Dirección de Calidad, dentro de los TREINTA (30) días
corridos de producida la modificación.
En cualquiera de estos casos, el laboratorio no podrá emitir
certificados hasta recibir la conformidad por parte de la Dirección de
Calidad.
Cualquier cambio posterior que se quiera realizar sobre el alcance de
habilitación deberá ser comunicado mediante nota y no surtirá efecto
hasta recibir la conformidad por parte de la Dirección de Calidad.
Toda modificación en el listado de equipamiento deberá ser informada
fehacientemente a la Dirección de Calidad dentro de los TREINTA (30)
días corridos de producida la modificación, mediante la presentación de
un nuevo Anexo I-D.
Otros cambios en los datos suministrados en cualquiera de los Anexos
presentados en el momento de la habilitación deberán ser informados
mediante la presentación de un nuevo Anexo actualizado al momento de la
Auditoría o a requerimiento de la Dirección de Calidad.
ARTÍCULO 14. — Para que proceda el cambio de Director Técnico, el nuevo
postulante al cargo deberá presentar toda la documentación requerida en
los Artículos 2° y 4° además de cumplir con los requisitos establecidos
en la presente resolución.
La presentación de la documentación no implicará la designación
automática del postulante en el cargo de Director Técnico, por lo que
el laboratorio no podrá emitir certificados suscriptos por el
postulante hasta recibir la conformidad por parte de la Dirección de
Calidad.
En casos de acefalía en la Dirección Técnica el laboratorio no podrá emitir certificados.
ARTÍCULO 15 — Los Laboratorios de Análisis Fitosanitarios de Papa
Semilla podrán habilitarse para realizar todos o parte de los ensayos
requeridos para las pruebas de post-control según la normativa vigente.
ARTÍCULO 16. — El INSTITUTO NACIONAL DE SEMILLAS podrá determinar la
realización de análisis de laboratorio para agentes fitopatógenos no
contemplados en la Resolución N° 217 de fecha 29 de octubre de 2002 o
la que en un futuro la reemplace en caso que lo considere necesario.
ARTÍCULO 17. — El Certificado de Habilitación Técnica emitido por la
Dirección de Calidad deberá estar expuesto al público junto a la
constancia de inscripción del Registro Nacional del Comercio y
Fiscalización de Semillas.
ARTÍCULO 18. — Queda prohibida en el ámbito nacional la actuación de
cualquier laboratorio que no cumplimente los requisitos establecidos en
la presente resolución.
La falta de inscripción en el Registro Nacional del Comercio y
Fiscalización de Semillas, hará pasible a los mismos de las sanciones
previstas en el Artículo 41 de la Ley N° 20.247.
ARTÍCULO 19. — El INSTITUTO NACIONAL DE SEMILLAS podrá advertir,
apercibir, suspender o dar de baja la habilitación técnica y/o la
inscripción del laboratorio en función de la ponderación de la gravedad
de las siguientes faltas:
a) Incumplimiento de deberes y obligaciones emergentes de la presente norma.
b) Impedir la realización de auditorías, o que en las mismas se
detecten reiteradas irregularidades, o ante el no levantamiento de las
“no conformidades” detectadas dentro del plazo estipulado por el
INSTITUTO NACIONAL DE SEMILLAS.
c) Falsedad en la información y datos suministrados.
ARTÍCULO 20. — Los conceptos y casos no previstos en la presente
normativa serán evaluados y resueltos por el INSTITUTO NACIONAL DE
SEMILLAS.
ARTÍCULO 21. — Derógase la Resolución N° 164 de fecha 28 de septiembre de 2004 y toda otra norma que se oponga a la presente.
ARTÍCULO 22. — Los Laboratorios de Análisis Fitosanitarios de Papa
Semilla que se encuentren vigentes en el Registro Nacional del Comercio
y Fiscalización de Semillas al momento de la publicación de la presente
resolución en el Boletín Oficial tendrán un plazo de SEIS (6) meses
para adecuarse a lo establecido en esta normativa.
ARTÍCULO 23. — Comuníquese, publíquese, dése a la Dirección Nacional
del Registro Oficial y oportunamente archívese. — Ing. Agr. RAIMUNDO
LAVIGNOLLE, Presidente del Directorio, Instituto Nacional de Semillas.
ANEXO I-A

ANEXO I-B

ANEXO I-C

ANEXO I-D
ANEXO I-E

ANEXO II-A
PROTOCOLO PARA ANÁLISIS VIROLÓGICO PARA TÉCNICA ELISA Y DOCUMENTO DE ADOPCIÓN DEL MÉTODO
PROTOCOLO
Los laboratorios deberán enviar a la Dirección de Calidad del INSTITUTO
NACIONAL DE SEMILLAS el protocolo utilizado para el análisis virológico
que realizan y su respectivo documento de adopción del método. Cada vez
que se introduzca un cambio en el protocolo el laboratorio deberá
redactar un nuevo documento de adopción del método (por ejemplo: cambio
de marca de anticuerpos y de marca de placas) y cumplimentar lo
establecido en el Artículo 13 de la presente resolución.
DOCUMENTO DE ADOPCIÓN DEL MÉTODO
Los protocolos aplicados para los análisis que se realizan en el
laboratorio deben haber sido ensayados de manera previa a su
aplicación, debido a que es necesario que el laboratorio demuestre que
domina el ensayo y lo realiza correctamente.
Como evidencia de los ensayos realizados el laboratorio deberá elaborar
un documento de adopción del método que deberá contener al menos:
- Objetivo y alcance del ensayo.
- Item a ensayar.
- Detalle de insumos, reactivos, materiales de referencia y acondicionamiento de las muestras.
- Listado de equipamiento necesario para su aplicación.
- Parámetros a evaluar:
1) Repetibilidad: proximidad entre los resultados de mediciones
sucesivas del mismo mesurando, realizadas bajo las mismas condiciones
de medición. (Aplicación de un mismo procedimiento, a un mismo objeto,
por el mismo analista, en intervalos cortos de tiempo, con el mismo
equipamiento, instrumental, en el mismo lugar).
2) Reproducibilidad: proximidad entre los resultados de mediciones de
un mismo mesurando, realizadas bajo distintas condiciones de medición.
(Aplicación de un mismo mesurando a diferentes analistas, distinto
equipamiento, intervalos largos de tiempo).
3) Límite de detección: menor concentración de analito en una muestra
de ensayo que puede ser confiablemente distinguida del blanco.
4) Robustez: capacidad de un método analítico para que los resultados
no se vean afectados por variaciones deliberadas en los parámetros del
procedimiento.
5) Especificidad/Selectividad: aseguran la confiabilidad de la medición del analito en presencia de interferencias.
6) Intervalo de trabajo/Linealidad: El ámbito de trabajo de un método
analítico es el intervalo entre los niveles más bajo y más alto de
concentraciones que ha sido demostrado que puede ser determinado con la
precisión y la exactitud requeridas para una determinada matriz (para
ensayos cuantitativos).
- Resultados obtenidos.
- Personas que desarrollaron los ensayos.
- Conclusiones, criterios de aceptación o rechazo del ensayo.
El laboratorio deberá decidir qué parámetros deberá evaluar en función del tipo de ensayo que realice.
El laboratorio deberá adjuntar el protocolo para la brotación con su
respectivo documento de adopción del método donde debe constar al menos
lo siguiente:
- Objetivo y alcance del ensayo.
- Item a ensayar.
- Detalle de insumos, reactivos, materiales de referencia y acondicionamiento de las muestras.
- Listado de equipamiento necesario para su aplicación.
- Resultados obtenidos.
- Personas que desarrollaron los ensayos.
- Conclusiones, criterios de aceptación o rechazo del ensayo.
PRESENTACIÓN - Requisitos de Forma
Tanto los Protocolos como sus Documentos de Adopción del Método deberán
ser presentados ante la Dirección de Calidad debiendo constar —además
de las especificaciones técnicas anteriormente mencionadas— todos los
datos identificatorios del Laboratorio y Director Técnico para su
correcta individualización, como asimismo, estar sellados y firmados
por el Director Técnico en cada una de sus hojas.
ANEXO II-B
PROTOCOLO PARA ANÁLISIS NEMATOLÓGICOS Y DOCUMENTO DE ADOPCIÓN DEL MÉTODO
PROTOCOLO
El laboratorio deberá utilizar el protocolo establecido en el Anexo III
de la presente normativa. Deberá elaborar un documento de adopción del
método para demostrar que los ejecutores de los ensayos dominan el
método de manera adecuada.
DOCUMENTO DE ADOPCIÓN DEL MÉTODO
El protocolo aplicado para los análisis que se realizan en el
laboratorio debe haber sido ensayado de manera previa a su aplicación.
Este documento debe contener al menos:
- Objetivo y alcance del ensayo.
- Item a ensayar.
- Detalle de insumos, reactivos, materiales de referencia y acondicionamiento de las muestras.
- Listado de equipamiento necesario para su aplicación.
- Resultados obtenidos.
- Personas que desarrollaron los ensayos.
- Conclusiones, criterios de aceptación o rechazo del ensayo.
PRESENTACIÓN - Requisitos de Forma
Tanto el Protocolo como el Documento de Adopción del Método deberán ser
presentados ante la Dirección de Calidad debiendo constar —además de
las especificaciones técnicas anteriormente mencionadas— todos los
datos identificatorios del Laboratorio y Director Técnico para su
correcta individualización, como asimismo, estar sellados y firmados
por el Director Técnico en cada una de sus hojas.-
ANEXO III
NORMAS DE FUNCIONAMIENTO DE LABORATORIOS DE ANÁLISIS FITOSANITARIOS DE PAPA SEMILLA
DISPOSICIONES GENERALES:
GENERALIDADES:
El alcance de la presente normativa es referente a los diagnósticos
obligatorios de enfermedades y nematodes transmitidos a las distintas
categorías y subcategorías de papa semilla.
Los laboratorios deberán contar con las condiciones ambientales,
físicas y de equipamiento necesarias para el desarrollo de sus tareas,
y podrán realizar sólo los ensayos para los cuales el INSTITUTO
NACIONAL DE SEMILLAS los haya habilitado.
Dichos ensayos deberán estar documentados en Protocolos con sus
respectivos documentos de adopción del método. Estos documentos deberán
ser presentados ante la Dirección de Calidad para su aprobación.
Cualquier modificación posterior implicará la necesidad de un nuevo
protocolo con su respectivo documento de adopción del método.
Asimismo, se recomienda que se tengan en cuenta las normas de higiene y
seguridad y aquéllas referidas al descarte seguro de residuos del
laboratorio.
El Director Técnico deberá capacitar a los analistas dejando la debida
constancia de dicha capacitación en el legajo del personal.
INSTALACIONES:
El área del laboratorio y cada una de sus dependencias debe ser
compatible con el volumen de muestras que se procesen y con el personal
disponible. Se debe establecer una separación eficaz entre zonas
vecinas cuando se desarrollen en ellas actividades incompatibles de
forma que el acceso y el uso de todos los sectores sea definido y
controlado. Estos sectores estarán detallados en un croquis en escala
que deberá presentarse al momento de la solicitud de habilitación.
En función del o los análisis para los cuales el laboratorio desee estar habilitado se deberá disponer de:
• Sector de recepción e ingreso de muestras (independiente de los demás sectores).
• Sector de acondicionamiento y lavado de muestras.
• Sector de brotación: debe contar con temperatura y humedad adecuadas,
con suficiente espacio para almacenar y acondicionar las muestras a
analizar.
• Sector para el análisis de virus.
• Sector para análisis de nematodes.
• Sector para análisis físico, morfológico y fisiológico.
• Sector para almacenamiento de drogas.
• Sector para almacenamiento de materiales de vidrio y plástico.
• Sector para el lavado de material.
• Sector de archivo de muestras.
• Sector de oficina.
EQUIPAMIENTO Y MATERIALES DE REFERENCIA:
El laboratorio deberá estar provisto de todos los equipos y materiales
de referencia necesarios para la correcta ejecución de los ensayos.
Cada equipo deberá tener una ficha técnica que contenga toda la
información necesaria del mismo, así como mantenimientos y
calibraciones realizadas. Todos los equipos deberán ser mantenidos en
adecuado estado de funcionamiento, debiendo para ello elaborarse un
plan de mantenimiento de los mismos.
El material de referencia deberá estar debidamente identificado con las características técnicas que se consideren relevantes.
PROCEDIMIENTOS, REGISTROS Y DOCUMENTOS:
El laboratorio deberá mantener un sistema documental en el que consten los siguientes registros:
• Protocolo de brotación y documento de adopción del método.
• Protocolo de análisis virológico y documento de adopción del método.
• Registro de pruebas periódicas de dilución de anticuerpos utilizados.
• Protocolo de análisis nematológico y documento de adopción del método.
• Registro de ingreso de muestras.
• Registro de brotación.
• Registro de análisis de virus (incluye boletín interno de análisis, lectura de lector ELISA/fotografías de placas).
• Registro de análisis de nematodes (boletín interno de análisis).
• Certificados de análisis emitidos.
• Registro de reactivos (facturas y/o remitos, fichas informativas que acompañan a los reactivos).
• Registro de equipos (listado de equipos, plan de mantenimiento, registros de controles, fichas técnicas).
• Registro de materiales de referencia.
Registro de ingreso de muestras: se registrarán en él todas las
muestras que ingresen al laboratorio, se haya emitido certificado o no,
con número correlativo (muestras de control interno de calidad,
particulares, entrenamiento, test de referencia, muestras de
fiscalización y otras). Los campos mínimos obligatorios que debe
contener este registro y que deben ser completados son: número de
muestra, código, peso del lote, fecha de recepción, remitente,
procedencia u origen, especie, estado de la muestra, número de
tubérculos enviados, fecha de inicio y final del análisis, fecha de
emisión del certificado de análisis.
Registro de análisis (de virus y nematodes): se elaborará un registro
de análisis por cada muestra el cual deberá estar identificado con el
mismo número de entrada que posee la muestra en el registro de ingreso
de muestras.
El registro de análisis deberá contar con la siguiente información:
número de ingreso de la muestra, determinaciones solicitadas, fecha de
inicio y finalización del análisis, resultados obtenidos, metodología
utilizada, datos e identificación del analista (si las etapas fueran
desarrolladas por distintos analistas, cada uno deberá indicar la etapa
que le corresponda mediante firma y aclaración o sus iniciales). Se
recomienda dejar un espacio para anotar observaciones que hubiera del
ensayo.
Informe de los resultados: los resultados de los ensayos solicitados se
informarán en el “Certificado de Sanidad de Papa Semilla” (Anexo IV).
Los resultados de virus y nematodes se informarán con una sola cifra
decimal (cuando el centésimo sea igual o superior a 5, el décimo
informado será el inmediato superior; si el centésimo es inferior a 5,
el décimo será el obtenido en el cálculo). Para el informe de mosaico
rugoso (PVX PVY) se sumarán aquellos pocillos en los que ambas
determinaciones resultaron positivas en la determinación individual de
las mismas.
Los análisis físicos, morfológicos y fisiológicos se informarán en el Certificado en el punto “Otros Ensayos”.
Archivo de Registros y Documentos:
Todos los registros, documentos y certificados emitidos deberán guardarse por un plazo de CINCO (5) años.
MUESTRAS PARA ANÁLISIS:
Las muestras recibidas deben ser identificadas con su respectivo número de ingreso.
Se deberán procesar como mínimo OCHENTA Y CINCO (85) de cada CIEN (100) tubérculos ingresados.
Una vez que ingresan al laboratorio deben procesarse en el menor tiempo
posible. En caso de no poder analizar las muestras inmediatamente,
deberán conservarse en lugar seco y ventilado para evitar alteraciones
en la calidad de las mismas.
La temperatura de conservación de las muestras no debe ser mayor a 15°
C y se deberán desechar los tubérculos que lleguen en mal estado.
Las muestras quedarán a total disposición del INSTITUTO NACIONAL DE
SEMILLAS, durante VEINTE (20) días corridos después de entregado el
correspondiente Certificado de Análisis, lapso durante el cual deberán
mantenerse en condiciones adecuadas de temperatura y humedad y
protegidas de contaminaciones. Se deberá garantizar la presencia de por
lo menos el brote apical.
ANÁLISIS FÍSICO, MORFOLÓGICO Y FISIOLÓGICO:
La muestra a analizar se deberá lavar previamente y luego se someterá
al análisis de síntomas visuales determinando los defectos externos
según la tabla de Tolerancias de Anormalidades de la normativa vigente.
ANÁLISIS VIROLÓGICOS:
1) Equipamiento:
• Micropipetas de volúmenes variables o varias de volúmenes fijos.
• Peachímetro rango de pH de 0 a 14, resolución 0,01, error +/- 0,1.
• Estufa de cultivo de temperatura regulable.
• Sistema de extracción de jugo de las muestras: mecánico (extractor /
dispensador de jugo de papa) o manual con bolsas de plástico.
• Balanzas analíticas, capacidad 120 gr., precisión 0,001 gr.
• Heladera y Freezer (-20° C).
• Equipo para producción de agua destilada o similar (o en su defecto deberá contar con agua destilada).
• Lector de microplaca (espectrofotómetro 405 nm) o cámara fotográfica y freezer.
Nota:
De optar por la cámara fotográfica y el freezer, la foto de la placa
deberá garantizar la correcta identificación de los testigos positivos,
sanos y blancos, permitir visualizar el resultado en cada celda y el
número identificatorio del análisis.
Las placas deberán conservarse en freezer de -20° C por un plazo de UN (1) año calendario.
2) Reactivos:
Los distintos reactivos empleados en los análisis de rutina deberán
estar rotulados con: fecha de apertura del envase y fecha de
vencimiento. Si se trata de soluciones preparadas en el laboratorio
(como buffers), el rótulo deberá tener los siguientes datos: nombre de
la solución, fecha de preparación, fecha de vencimiento, pH y nombre
del analista que preparó la misma.
3) Material de Referencia:
• Testigos positivos.
• Testigos sanos.
• Blanco (Buffer).
El laboratorio deberá contar con los testigos positivos y sanos adecuados para conducir los ensayos.
Asimismo, deberá tener en cuenta que la intensidad de la reacción puede
cambiar según la variedad. Por lo tanto, se recomienda tener testigos
positivos y sanos acordes a la variedad de la muestra a analizar al
momento de la adopción del método.
4) Tratamiento de brotado de papa:
Los tubérculos de papa debidamente identificados serán sometidos a un
proceso para promover la brotación según el protocolo que utilice el
laboratorio. Este protocolo deberá estar avalado por el documento de
adopción del método.
En el registro de brotación se deberá indicar la fecha de inicio del
proceso, control de temperatura en el recinto, fecha de finalización
del proceso y porcentaje de tubérculos brotados.
No podrá realizarse el análisis virológico hasta que transcurran 3
semanas desde el inicio de la ruptura de dormición. Para realizar los
análisis es necesario que los tubérculos estén uniformemente brotados.
Se deberá utilizar 1 brote de cada tubérculo procesado.
5) Técnica ELISA:
El protocolo empleado dependerá de la marca comercial del kit utilizado
por el laboratorio: debiendo el mismo estar documentado y adoptado. Se
deberán tener en cuenta las siguientes consideraciones:
• La extracción se realizará a partir de brotes, hojas o tubérculos
brotados según el protocolo empleado por el laboratorio, con una
dilución previamente determinada (habitualmente se utilizan 20 ml de
solución de extracción por cada gramo de tejido vegetal).
• Prueba de diluciones de anticuerpos: se realizará cada vez que se
abre un nuevo lote de anticuerpos y deberá emplearse un positivo de
baja concentración.
• Emplear el brote apical, (para el caso del PLRV, cuanto más cerca se
esté de la cosecha, se deberán emplear brotes de la zona del ombligo).
• Sólo se permitirá el uso de anticuerpos policlonales.
• El número de testigos a emplear por placa, será como mínimo, el siguiente:
- testigos positivos (enfermos): 2. Uno de la menor concentración
posible tal que se distinga del testigo sano y otro de una
concentración mayor.
- testigos negativos (sanos): 3.
- blanco (buffer): 1.
• El agregado de azida sódica a los buffers permite su conservación
durante 2 meses. En caso contrario, se deberán usar dentro de las 24
horas.
• El uso de leche descremada permite eliminar riesgos de reacciones
inespecíficas. Su uso en el buffer conjugado es particularmente útil
para PLRV.
6) Interpretación de resultados:
El tiempo de lectura variará según la calidad de las placas usadas, del
virus analizado y de los anticuerpos empleados. Se podrá hacer una
lectura preliminar a los 30 minutos y la lectura final deberá ser a los
60 minutos.
En cuanto a la lectura visual, se considerará muestra positiva a
aquella que presente una coloración amarilla igual o superior a la del
testigo positivo de menor concentración; y muestra negativa a la que
tenga una coloración igual o menor a la del testigo sano.
En lo que respecta a las lecturas con lector de microplacas, se
considerarán muestras positivas a aquellas cuyas lecturas de
absorbancia a una longitud de onda de 405 nm (A405) sean superiores a
la media de los 3 testigos sanos, más 3 veces el desvío estándar. Todas
las muestras con valores de absorbancia menores a lo expresado serán
consideradas sanas.
En caso de lecturas donde el cálculo arroje interpretaciones dudosas o
confusas, la interpretación final de los resultados quedará a criterio
del Director Técnico.
ANÁLISIS NEMATOLÓGICO:
1) Equipamiento:
• Microscopio óptico (35X a 100X).
• Centrífuga (dependiendo del método empleado).
• Licuadora eléctrica.
• Tamices de distintas tramas.
• Balanza analítica.
2) Determinación de Nacobbus aberrans y Meloidogyne sp.
La muestra deberá ser dividida en grupos de no más de 20 papas. Se
deberá pelar sólo la mitad de cada papa. Si en alguno de estos grupos
se encontrara más de un individuo, se deberá volver a la muestra y
analizar papa por papa (que conserva una mitad sin pelar), ya que los
resultados de Nacobbus aberrans y de Meloidogyne sp. deben expresarse
en porcentaje.
Procedimiento:
Una vez ingresada la muestra de tubérculos, se realizará una inspección
visual para separar los tubérculos con síntomas visibles, dudosos y
aparentemente sanos colocándolos en canastos aireados. Eliminar la
tierra y restos orgánicos de los tubérculos, dejando la superficie
limpia de todo elemento extraño. Se podrá realizar la observación del
material dilacerando bajo microscopio óptico tejidos con síntomas
visibles de agallas o presencia de zonas necróticas.
Se procederá al pelado de los tubérculos (2 mm de profundidad),
empleando un utensilio filoso para una mejor extracción de la epidermis.
Se pesarán entre 20 a 40 gramos de las pelas y se licuarán,
incorporando 200 ml de agua y 2 ó 3 gotas de detergente (10 a 90
segundos, según sea la velocidad del aparato).
Se trasvasará y decantará durante 3 minutos (o se dejará decantar en la licuadora), eliminando el sobrenadante.
Se procederá luego a tamizar el material, empleando un colador y una
batería de tamices de malla N°: 60, 270, 300 y 325, descartando el
material del colador y el del tamiz de malla N° 60. Se trasvasará el
contenido del último tamiz (de malla N° 325) con una fina lluvia de
agua a un vaso de precipitado. Luego se procederá a la evaluación,
pudiendo utilizarse el método de evaluación directa o indirecta según
se requiera.
Evaluación directa: se colocará el material en una caja de petri,
procurando observar cada vez 2 a 3 cm3 de suspensión, volumen
suficiente para cubrir con una delgada capa el fondo de la misma. Este
pequeño volumen facilitará una mejor transparencia de la suspensión
para la observación y recuento de los nematodes extraídos bajo
microscopio óptico.
En caso de existir abundancia de gránulos de almidón, que impidan la
correcta evaluación, hervir la solución durante 1 a 3 minutos. También
es posible la coloración del material y su posterior observación
directa bajo microscopio óptico.
Evaluación indirecta: se centrifugará el material transfiriendo el
contenido del vaso de precipitado al interior de los tubos de la
centrífuga, siendo conveniente el agregado de 10 gr. de kaolín, a fin
de favorecer la sedimentación de los elementos más pesados que el agua
(nematodes y fase mineral). La duración de este centrifugado será de 4
minutos a 3000 rpm. El sobrenadante obtenido (materia orgánica y agua)
será desechado.
Al sedimento resultante de la primera centrifugación se le agregará una
cierta cantidad (que varía en función de la capacidad de los tubos de
centrífuga empleada), de solución azucarada de densidad 1,18 (60%), el
sedimento es totalmente disgregado con ayuda de un agitador a fin de
lograr una buena suspensión del primero en la solución azucarada. Se
realizará una segunda centrifugación con el objeto de obtener una
solución límpida en la cual sea fácil observar los nematodes. Se
realizará un centrifugado de 1 minuto a 1800 rpm. Los nematodes
quedarán en suspensión en el sobrenadante. Rápidamente se pasará el
sobrenadante por el tamiz de malla N° 325 y se transferirán los
nematodes a una caja de petri u otro recipiente con ayuda de una fina
lluvia de agua. Esta operación deberá ser rápida para evitar que los
nematodes se plasmolicen. La solución resultante será límpida y los
nematodes podrán ser observados bajo microscopio óptico.
ANEXO IV
e. 16/11/2015 N° 166507/15 v. 16/11/2015

